Статьи
Золотая защита: учёные изобрели способ уменьшить побочное действие лучевой терапии
Российские учёные создали новую систему доставки радионуклидов к раковой опухоли. Им удалось снизить побочное воздействие радиоактивного изотопа благодаря плёнке из золота или титансодержащего органического соединения. Испытания на мышах показали, что новый способ позволяет заблокировать нетерапевтическое излучение на 98%. Это позволит значительно уменьшить побочные эффекты лучевой терапии.
Группа учёных из Российского научного центра радиологии и хирургических технологий им. академика А.М. Гранова, Санкт-Петербургского политехнического университета Петра Великого, Национального исследовательского университета ИТМО и Национального исследовательского Томского политехнического университета разработала новую, более безопасную систему доставки радиоактивных изотопов к раковой опухоли. Проект получил грант Российского научного фонда. Результаты опубликованы в журнале Journal of Colloid and Interface Science.
Новая методика способна снизить побочную дозу радиации до 2%. Существующие сейчас способы позволяют добиться снижения этого излучения только до 16% от общего объёма введённых в организм пациента радиоактивных изотопов.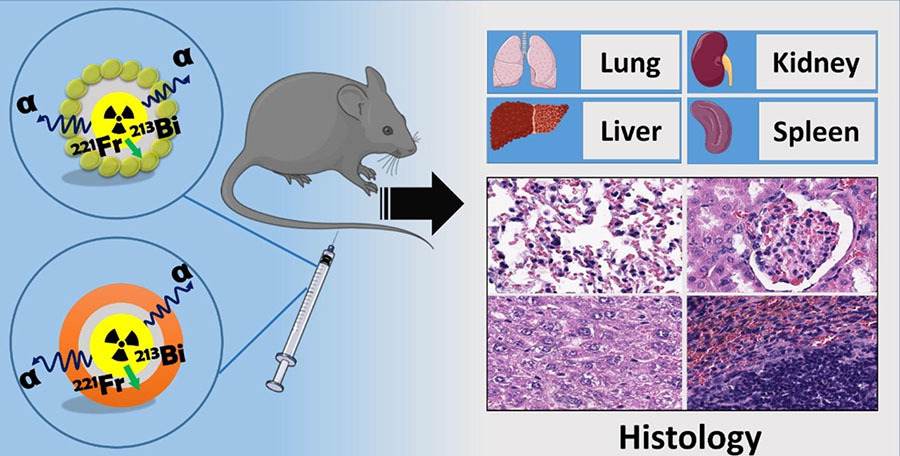
- Схема эксперимента
- © Источник: Karpov et al. / Journal of Colloid and Interface Science.
В качестве терапевтического вещества исследователи выбрали радионуклид актиния-225 (225Ac). Как объяснили учёные, во-первых, при его распаде образуется достаточно энергии для эффективного воздействия на раковые клетки. Во-вторых, изотоп обладает достаточным для транспортировки в медицинские учреждения периодом полураспада — его активность снижается вдвое за десять суток. Этот радионуклид применяется в ядерной медицине, а российская госкорпорация «Росатом» даже экспортирует актиний-225 за рубеж.
Для доставки радиоактивного изотопа к опухоли российские учёные разработали и синтезировали наночастицы диоксида кремния. Затем к наночастицам химически присоединили радионуклиды и сверху покрыли плёнкой из золота или титансодержащего органического соединения.
«Именно эти дополнительные слои должны были предотвратить отсоединение актиния-225 и его дочерних изотопов от частиц-носителей и их хаотичное циркулирование по организму, приводящее к повреждению здоровых тканей и органов», — говорится в пресс-релизе Российского научного фонда.
Эффективность изобретения исследователи проверили на лабораторных мышах. Одной группе животных ввели новый препарат в форме суспензии, второй — чистый актиний-225 без наночастиц-носителей или с наночастицами, но без покрытия из золота или титана.
«Оказалось, что во всех контрольных вариантах уже на третий день радионуклид накапливался в печени, селезёнке и почках, приводя к отмиранию клеток этих органов. Напротив, наночастицы с актинием-225, дополнительно покрытые слоем золота или титана, практически не вредили здоровым тканям даже через десять суток», — отмечают авторы исследования.
Учёным удалось установить, что новая система доставки радионуклида способна удерживать более 98% изотопов.
Как рассказал RT один из авторов изобретения, сотрудник группы нанофармакологии лаборатории генной инженерии Российского научного центра радиологии и хирургических технологий им. академика А.М. Гранова Тимофей Карпов, разработка позволит безопасно доставлять радионуклиды к опухолям, не нанося вреда здоровым тканям организма.
- Клетки раковой опухоли
- Gettyimages.ru
- © koto_feja
«Помимо исследований на лабораторных животных, мы провели in vitro эксперименты — «в пробирке», — которые доказали, что синтезированные нами частицы удерживают актиний-225 и его дочерние изотопы от вытекания на протяжении 30 дней», — пояснил учёный.
На следующем этапе работы исследователи планируют модифицировать поверхность наночастиц с помощью особых молекулярных «меток». Это придаст препарату избирательность — попав в организм, он будет мигрировать к раковым клеткам.
Лечебный атом
Лучевая терапия позволяет эффективно бороться с онкологическими заболеваниями. Во время радионуклидной терапии радиоактивные изотопы вводятся в организм пациента либо практически в чистом виде, либо в составе комплексных препаратов.
Энергия ионизирующего излучения разрушает как сами клетки раковой опухоли, так и их ДНК, благодаря чему они теряют способность к делению. За счёт специальных молекулярных «меток» радионуклиды действуют целенаправленно, скапливаясь только в месте опухоли.
Однако метод имеет серьёзный недостаток: пока радионуклид достигнет своей цели, ионизирующее излучение успевает нанести вред и здоровым органам. Чтобы нейтрализовать этот эффект, разработчики препаратов для лучевой терапии применяют специальные носители, «удерживающие» радионуклид и продукты его распада до момента их доставки к опухоли. Обычно для этого используются короткие белковые молекулы, искусственные мембранные пузырьки, а также наночастицы из неорганических соединений.